Резюме
Актуальність. Проблема ревізійного ендопротезування в сучасній ортопедії стоїть надзвичайно гостро, про що свідчить збільшення його частоти. Проте ймовірні фактори, що призводять до розвитку нестабільності компонентів ендопротеза колінного суглоба, за даними різних авторів, різняться, потребують вдосконалення і методи оцінки результатів ендопротезування. Мета: визначити фактори ризику, що вплинули на результати ендопротезування колінного суглоба, та запропонувати методику оцінки результатів ендопротезування. Матеріали та методи. Робота ґрунтується на аналізі результатів лікування 105 протезованих хворих. Операції виконані за період з 2010 по 2021 рік на базі клініки ортопедії та травматології дорослих ДУ «Інститут травматології та ортопедії НАМН України». Проводилось клініко-анамнестичне обстеження пацієнтів з визначенням індексу маси тіла, супутньої патології та умов праці, осі прооперованої кінцівки, визначались ранні післяопераційні ускладнення та фактори, що призводять до тугорухомості суглоба, проводилось рентгенографічне (з визначенням перипротезних зон лізису кісткової тканини) та сонографічне дослідження. Дані, отримані в результаті обстеження, статистично оброблені. Результати. Встановлено фактори ризику, що вплинули на нестабільність компонентів ендопротеза колінного суглоба: важка фізична праця (t = 1,34 і вище, р < 0,05); ожиріння зі значенням ІМТ ≥ 30 (t = 2,24 і вище, р < 0,05), залишкова деформація (хi2 = 4,55, n = 2, р < 0,05); ранні післяопераційні ускладнення (Z = 7,25, p < 0,01), порушення техніки цементування стегнового (t = 1,63 і вище, р < 0,05) та великогомілкового компонентів (t = 1,36 і вище, р < 0,05). Серед ранніх факторів ризику виділено: резорбцію кісткової тканини на межі «цемент — кістка» у вигляді смужки просвітлення (з локалізацією в 1, 2, 3, 4-й зонах за Hyojeong Mulcahy і Felix S. Chew) в дистальному відділі стегнової кістки (t = 4,95 і вище, р < 0,05), проксимальному відділі великогомілкової кістки (t = 1,52 і вище, р < 0,05), динамічна проба на нестабільність та УЗД-критерії діагностики розхитування (ознаки гіперваскуляризації, синовіт з об’ємом рідини понад 50 см3). Серед пізніх факторів ризику нестабільності визначено зміни на межі «цемент — кістка» і «імплант — цемент», з локалізацією в «зонах виступів» (5-та, 6-та, 7-ма зони за Hyojeong Mulcahy і Felix S. Chew) в ділянці стегнової (t = 1,63 і вище, р < 0,05) та великогомілкової кісток (t = 1,36 і вище, р < 0,05). Факторами, що вплинули на розвиток тугорухомості в протезованому суглобі, були: оперативні втручання до ендопротезування (t = 1,53 і вище, р < 0,05), ранні ускладнення (t = 1,49 і вище, р < 0,05), супутні захворювання в анамнезі (хi2 = 4,55, р < 0,05), пошкодження зв’язкового апарату (хi2 = 7,55, р < 0,05), судин, нервів під час ендопротезування (хi2 = 6,55, р < 0,05), залишкові деформації осі кінцівок (хi2 = 4,55, р < 0,05). Висновки. На основі вивчених факторів, що вірогідно вплинули на результати ревізійних операцій, запропоновано системний підхід до оцінки результатів ревізійного ендопротезування колінного суглоба, що дозволить уникнути післяопераційних ускладнень та поліпшить якість лікування цієї складної категорії хворих.
Background. The problem of revision arthroplasty in modern orthopedics is extremely acute, as evidenced by an increase in its frequency. However, the probable factors that lead to the development of instability of the knee endoprosthesis components, according to various authors, differ among themselves, and the methods for evaluating the outcomes of arthroplasty require improvement as well. The purpose was to determine the risk factors that affected the outcomes of knee replacement, and to propose a methodology for assessing the latter. Materials and methods. The work is based on the analysis of treatment outcomes in 105 prosthetic patients. The operations were performed from 2010 to 2021 at the basis of the clinic for orthopаedics and traumatology of adults at the State Institution “Institute of Traumatology and Orthopаedics of the National Academy of Medical Sciences of Ukraine”. A clinical and anamnestic examination of patients was carried out with evaluation of the body mass index, concomitant pathology, and working conditions, the axis of the operated limb, early postoperative complications and factors leading to joint stiffness; radiographic (with the determination of periprosthetic bone tissue lysis zones) and sonographic examination was conducted. The data obtained are statistically processed. Results. The risk factors that influenced the instability of knee endoprosthesis components were as follows: heavy physical work (t = 1.34 and higher, p < 0.05); obesity with body mass index ≥ 30 (t = 2.24 and above, p < 0.05), residual deformity (хi2 = 4.55, n = 2, p < 0.05); early postoperative complications (Z = 7.25, p < 0.01), violation of cementing technique for the femoral (t = 1.63 and higher, p < 0.05) and tibial component (t = 1.36 and above, p < 0.05). Among the early risk factors, there are resorption of bone tissue at the cement-bone interface in the form of a light strip (with location in zones 1, 2, 3, 4 according to Hyojeong Mulcahy and Felix S. Chew) in the distal femur (t = 4.95 and higher, p < 0.05), the proximal tibia (t = 1.52 and above, p < 0.05), dynamic test for instability and ultrasound criteria for loosening (signs of hypervascularization, synovitis with a fluid volume of more than 50 cm3). Among the late instability risk factors, we identified changes at the cement-bone and implant-cement interface, with localization in the protrusion zones (5, 6, 7 according to Hyojeong Mulcahy and Felix S. Chew) in the femoral (t = 1.63 and higher, p < 0.05) and tibial areas (t = 1.36 and above, p < 0.05). The factors that influenced the development of stiffness in the prosthetic joint were operative interventions before arthroplasty (t = 1.53 and higher, p < 0.05), early complications (t = 1.49 and above, p < 0.05), concomitant diseases in the past medical history (хi2 = 4.55, p < 0.05), damage to the ligaments (хi2 = 7.55, p < 0.05), nerves, vessels during arthroplasty (хi2 = 6.55, p < 0.05), residual deformities of the limb axis (хi2 = 4.55, p < 0.05). Conclusions. Based on the studied factors that probably influenced the results of revision surgeries, a systematic approach to the evaluation of the outcomes of revision knee replacement is proposed, which will help avoid postoperative complications and improve the quality of treatment of this complex category of patients.
Вступ
Загальновідомо, що тотальне ендопротезування колінного суглоба (ТЕКС) є ефективним методом лікування пацієнтів з дегенеративно-дистрофічними захворюваннями в їх термінальних стадіях та наслідками травм колінного суглоба [1]. Зведена статистика виживання ендопротезів колінного суглоба становить близько 82 % протягом 12 років, а добрі та відмінні результати спостерігаються протягом 50–80 % цього терміну [2]. Проте проблема ревізійного ендопротезування в сучасній ортопедії стоїть надзвичайно гостро, про що свідчить збільшення його частоти [3]. Найбільш частою причиною ревізійного протезування є інфекційні ускладнення та розхитування компонентів або їх комбінація, що сумарно становлять близько 60 % від усіх ускладнень. Більшість невдач спостерігаються в перші 2 роки після операції, серед яких [4, 5]: парапротезна інфекція (25,2–44,1 % від усіх ускладнень); тугорухомість (22,6 % від усіх ускладнень); нестабільність компонентів (16,1 % від усіх ускладнень); нестабільність суглоба (2,9–13 % від усіх ускладнень); злам компонентів (9,7 % від усіх ускладнень); перипротезний остеоліз (3,2 % від усіх ускладнень); перипротезні переломи (1,5 % від усіх ускладнень); ТЕЛА, гетеротопічна осифікація, пошкодження розгинального апарату, пошкодження судин та нервів (2,2–5,7 % від усіх ускладнень).
Деякі дослідники [4, 6] вказують, що розхитування компонентів ендопротеза є однією з основних причин незадовільних результатів ТЕКС. Нестабільність може бути ранньою, внаслідок неналежної фіксації, та пізньою — у результаті остеолізу. Цементування компонентів забезпечує швидку і надійну їх фіксацію з подальшим позитивним клінічним ефектом, але тільки при чіткому дотриманні правил цементування. На особливу увагу заслуговують безцементні конструкції ендопротезів, завданням яких є можливість протезування відносно молодих пацієнтів з можливістю формування біологічної вторинної фіксації внаслідок вростання кісткової тканини в глибину покриття ендопротезів. Але на сьогодні відсутні переконливі дані, які б свідчили про перевагу безцементних конструкцій над цементними.
Слід зазначити, що надійно фіксований цементний ендопротез поступово може розхитатися. І це пов’язано з багатьма факторами, одним з ключових є неправильне просторове розміщення компонентів та балансування проміжків [7]. Як вказує Fang et al., функціональність і виживання протеза залежать від вирівнювання осі кінцівки [8]. Проаналізувавши результати великої кількості первинних протезувань з середнім терміном 6,6 року після операції, автори виявили статистично значуще збільшення випадків невдач у пацієнтів з вальгусним тибіофеморальним кутом у діапазоні 2,4–7,20. Це пов’язано з концентрацією напружень як безпосередньо на кістковій тканині, так і внаслідок дії продуктів зношення поліетилену, кількість яких значно зростає через ці концентрації. На зношення поліетилену впливає не лише вирівнювання осі, але й тиск між поверхнями стегнового та гомілкового компонентів, що контактують, механізм замикання лайнера та механізм замикання між компонентами у зв’язаних протезах з можливістю ротації чи без неї. Крім того, більшість хірургів вважають, що зношення залежить від фізичної активності та надмірної маси тіла пацієнта [9, 10]. Проте імовірні фактори, що призводять до розвитку нестабільності компонентів ендопротеза колінного суглоба, за даними різних авторів, різняться, потребують вдосконалення і методи оцінки результатів ендопротезування.
Тому цікавим у науковому та практичному сенсі вважаємо проаналізувати клінічний матеріал для розв’язання нагальних питань.
Мета дослідження: визначити фактори, що вплинули на результати ендопротезування колінного суглоба, з метою поліпшення якості лікування хворих.
Матеріали та методи
Робота основана на аналізі результатів 105 хворих після ендопротезування колінного суглоба. З них 85 пацієнтів з ревізійними ендопротезуваннями та 20 пацієнтів після проведеного ендопротезування колінного суглоба без клінічних ознак нестабільності компонентів ендопротеза (контрольна група при проведенні УЗ-дослідження). Операції виконані за період з 2010 по 2021 рік на базі клініки ортопедії та травматології дорослих ДУ «Інститут травматології та ортопедії НАМН України».
Розподіл хворих з нестабільними компонентами ендопротеза за статтю та віком наведено в табл. 1 та на рис. 1.
Абсолютну більшість становлять жінки віком 60–74 роки. Коефіцієнт кореляції Пірсона, який характеризує залежність кількості хворих з нестабільними компонентами ендопротеза від віку, дорівнює: 0,98 для чоловіків та 0,85 для жінок (табл. 1).
Клінічна частина обстеження передбачає виявлення скарг хворого на біль в оперованому суглобі та умови його виникнення, користування додатковою опорою. Встановлювали масу тіла хворого, тяжкість праці та супутні захворювання. Обов’язковим моментом є вимірювання довжини оперованої кінцівки та об’єму рухів в оперованому суглобі, визначення приросту відносного вкорочення порівняно з попереднім обстеженням. Для визначення стану прооперованого колінного суглоба користувались альгофункціональним індексом Лекена [11].
У діагностиці асептичного розхитування компонентів ендопротеза колінного суглоба ключову роль відіграють променеві методи діагностики. Так, рентгенологічними ознаками розхитування компонентів ендопротеза колінного суглоба є широкі (понад 2 мм) лінії просвітлення, що прогресують на межі «цемент — кістка» або «цемент — метал», міграція або просідання компонентів ендопротеза і злам цементної мантії [12].
Hyojeong Mulcahy та Felix S. Chew у 2014 році запропонували з метою більш точної оцінки контактних поверхонь імпланта, цементу та кістки розбивати рентгенограму на умовні зони (рис. 1, 2) [13].
У ДУ «Інститут травматології та ортопедії НАМН України» на базі відділу функціональної діагностики в період з 2010 по 2021 рік виконано 40 УЗ-досліджень протезованих хворих. У контрольній групі у 20 пацієнтів не було ні рентгенологічних, ні клінічних ознак асептичної нестабільності компонентів ендопротеза, у 20 інших пацієнтів мали місце клінічні ознаки асептичного розхитування ендопротеза. А саме: біль при навантаженні суглоба, обмеження функції. Вірогідних рентгенологічних ознак нестабільності в обох групах пацієнтів не було. Групи були вірогідно однорідні за віком та статтю.
Дослідження проводилось за допомогою ультразвукового апарата Simens Sonoline G-50 с лінійним датчиком 3–7,5 МГц. Частота вибиралася залежно від глибини припустимого процесу. Використовували стандартну методику дослідження, датчик встановлювали сагітально та фронтально щодо патологічного вогнища. Оцінювали наявність або відсутність рідини інтраартикулярно, її об’єм, розміри порожнини, яка вміщує рідину, ехогенність вмісту, наявність включень та рухливість компонентів. Також проводили функціональну пробу на наявність нестабільних компонентів ендопротеза. Хворий після дослідження лежачи згинав колінний суглоб під кутом 90 градусів, і виконувалось функціональне навантаження на протезований суглоб у фронтальній площині [14].
У своїй роботі ми користувалися класифікацією кісткових дефектів ложа нестабільного протеза колінного суглоба за AORI (Anderson Orthopaedic Research Institute, USA) [15].
Конституцію пацієнтів визначали за допомогою індексу маси тіла (ІМТ, індекс Кетле) [16]. Відповідність між масою та зростом людини за ІМТ трактується наступним чином: ІМТ менше за 18,5 — недостатня маса тіла; 18,5–24,9 — норма; 25–29,9 — ожиріння І ступеня; 30–39,9 — ожиріння ІІ ступеня; більше ніж 40 — ожиріння ІІІ ступеня.
Для проведення розрахунків користувалися базою даних обстеження хворих з ускладненнями після проведеного ТЕКС, що були введені в таблицю Microsoft Excel 2003. Статистичну обробку результатів проводили за допомогою загальноприйнятих методів (критерій Крускала — Уолліса, обчислення поліхоричного та тетрахоричного показника зв’язку, порівняння двох середніх) у програмних середовищах MS Excel 2010 та Statistica 12.6 (StatSoft). Перевірку гіпотези про нормальний розподіл проводили за допомогою моментів вищого порядку (асиметрії й ексцесу).
Результати та їх обговорення
З метою визначення факторів, що вплинули на результати ендопротезування колінного суглоба, та розробки методики оцінки результатів протезування проведено клініко-анамнестичне обстеження з визначенням супутньої патології, індексу маси тіла, показників тяжкості праці. З 85 обстежених пацієнтів у 73 % виявлено супутню патологію: ІХС була у 9 (10,6 %) хворих, гіпотиреоз — у 17 (20 %), гіперти–реоз — у 13 (15,3 %), цукровий діабет — у 23 (27 %). Щодо залежності нестабільності та маси тіла визначено вірогідне домінування випадків з ожирінням ІІІ ступеня. З ІМТ 18,5–24,9 було 18 (21,18 %), з ІМТ 25–29,9 — 24 (28,24 %), з ІМТ 30–39,9 — 36 (42,35 %), з ІМТ ≥ 40 — 7 хворих (8,24 %). Тобто надмірна маса тіла стала фактором, що призвів до виникнення нестабільності компонентів колінного суглоба (ІМТ ≥ 30, Z = 2,08, p < 0,05). Цей висновок подібний до результатів S. Gunst, M.H. Fessy (2015), які стверджують, що ризик реендопротезувань через асептичну нестабільність великогомілкового компонента вдвічі більший у пацієнтів з ІМТ ≥ 35 кг/м2, незалежно від віку чи розташування кінцівок [17].
Хворі, які звертались з нестабільністю ендопротеза, займались середньою та важкою працею. Середня важкість праці була у 21 пацієнта (24,71 %), важка праця була у 45 (52,94 %), залежність вірогідна (Z = 6,25, p < 0,01).
За типом попередніх оперативних втручань на суглобі випадки нестабільності компонентів розподілилися наступним чином: не було операцій у 51 випадку (60,0 %), МОС виростків стегнової чи великогомілкової кістки було виконано у 7 випадках (8,2 %), корекційну остеотомію стегнової чи великогомілкової кістки було виконано у 4 випадках (4,7 %), артроскопію (дебридмент, синовектомія, парціальна резекція меніска чи меніскектомія) — у 20 випадках (23,5 %), відкриту чи артроскопічну пластику хрестоподібних зв’язок було виконано у 3 випадках (3,5 %). Вірогідно домінували випадки без попередніх оперативних втручань (t = 5,15 і вище, р < 0,05). Аналогічне домінування випадків без операцій у групі з тотальною нестабільністю (t = 4,29 і вище, р < 0,05) — 63,0 %, з ізольованою нестабільністю (t = 1,52 і вище, р < 0,05) СК — 64,3 %, з ізольованою нестабільністю (t = 2,58 і вище, р < 0,05) ВК — 53,6 %. Отримані результати свідчать про те, що попередні оперативні втручання не є причиною розхитування стегнового та великогомілкового компонентів, оскільки більшість з них розхиталась саме у тих випадках, коли попередніх оперативних втручань на колінному суглобі не було (табл. 2). За даними J.B. Lim (2016), пацієнти з операціями на колінному суглобі в анамнезі мають такі ж післяопераційні результати, як і ті, хто раніше не оперувався [18].
/35.jpg)
У хворих з нестабільними ендопротезами мала місце значна кількість залишкових деформацій — 66 випадків, або 77,6 %. Таким чином, залишкові деформації осі кінцівки та позиція компонентів значно вплинули на успіх ендопротезування та стабільність компонентів. Залежність вірогідна з Z = 3,15, p < 0,01. Результати щодо високої частоти поєднання кісткових деформацій після ендопротезування колінного суглоба з нестабільністю ендопротезів узгоджуються з даними інших досліджень у цій галузі [19].
Визначали ранні ускладнення, що виникали протягом перших тижнів у хворих з нестабільними компонентами ендопротеза (табл. 3).
У хворих з нестабільними ендопротезами ранні ускладнення становили майже 94 %. Залежність вірогідна з Z = 7,25, p < 0,01. Тобто ранні післяопераційні ускладнення вплинули на розвиток нестабільності компонентів ендопротеза колінного суглоба. Дослідження Bozic et al. (2014) показало, що ранні ускладнення після тотального ендопротезування колінного суглоба, як-от інфекція, артрофіброз та нестабільність, є основними причинами ревізійних операцій. Автори виявили, що частота таких ускладнень може сягати 35 % [19].
Було досліджено розподіл випадків нестабільності за значенням об’єму рухів протезованого колінного суглоба в сагітальній площині (табл. 4).
Як видно з табл. 4, з усіх випадків розхитування компонентів вірогідну більшість (t = 9,5 і вище, р < 0,05) становили випадки нестабільності з повним обсягом рухів в оперованому суглобі, а саме 63 випадки, що становило 74,1 %. Повний об’єм рухів з ознаками перерозгинання спостерігався лише у 9 випадках (10,6 %), а тугорухомість зі згинально-розгинальними контрактурами було виявлено у 13 випадках (15,3 %). Причому повний обсяг рухів вірогідно домінував (t = 5,8 і вище, р < 0,05) як у групі з тотальною нестабільністю компонентів ендопротеза — 31 випадок (72,1 %), так і в групах з нестабільністю СК — 9 випадків, що становить 64,3 % (t = 1,52 і вище, р < 0,05), і нестабільністю ВК — 23 випадки, що становить 82,1 % (t = 6,79 і вище, р < 0,05).
За післяопераційними рентгенограмами визначали якість первинного цементування. Вимірювали площу контакту цементної мантії та кістки стегна і гомілки у відсотках (табл. 5).
Аналізуючи табл. 5, ми визначили пряму залежність зниження частки контакту цементу з кісткою менше ніж 70 % з невдачами ендопротезування (переважають випадки контакту 40–70 % площі — 31 % випадків). Тобто якість цементування значно вплинула на розвиток нестабільності компонентів ендопротеза. Залежність вірогідна з Z = 3,25, p < 0,01. Водночас дослідження Sharkey et al. (2014) показало, що недостатній контакт цементу з кісткою (40–70 %) був одним з основних факторів, що призводили до нестабільності компонентів ендопротеза після ревізійного ендопротезування колінного суглоба [20].
Вивчили також за рентгенограмами ознаки лізису, що прогресує понад 2 мм у зонах Hyojeong Mulcahy і Felix S. Chew, перелом цементної мантії та міграцію компонентів (табл. 6, 7).
Тобто визначено значну залежність наявності лізису, що прогресує понад 2 мм, у хворих з нестабільними стегновими компонентами ендопротеза — 100 % випадків. Переважав лізис у зонах 1, 2 та 5.
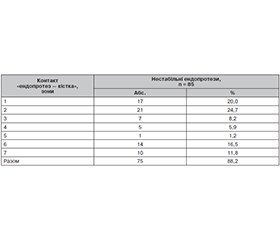
Визначено наявність лізису навколо нестабільного великогомілкового компонента ендопротеза у 75 хворих (88,2 % випадків). Домінував лізис у зонах 1, 2 (44,7 %) та 6, 7 (28,1 %) (табл. 7).
Таким чином, лізис кісткової тканини, що прогресує, навколо компонентів ендопротеза є причиною дестабілізації компонентів ендопротеза. Залежність вірогідна з Z = 6,25, p < 0,01. А ранніми ознаками дестабілізації є його прояви в зонах 1, 2 за Hyojeong Mulcahy і Felix S. Chew як на стегні, так і на гомілці. Sharkey et al. (2014) виявили, що у 60 % випадків з нестабільністю компонентів спостерігався значний лізис кістки. Автори наголошують на важливості ретельного рентгенологічного моніторингу для своєчасного виявлення ознак лізису та нестабільності [20].
Також провели УЗ-дослідження стабільних та нестабільних компонентів ендопротеза.
Визначено, що у хворих з нестабільними компонентами УЗ-ознаками нестабільності компонентів ендопротеза є ознаки гіперваскуляризації — 36 %, синовіт — 57,6 %, позитивна динамічна проба на нестабільність — 81,2 % та об’єм синовіальної рідини, у середньому більший ніж удвічі. Залежності вірогідні, p < 0,01 (табл. 8).
Таким чином, УЗ-ознаки нестабільності та зниження функціональної бальної оцінки менше від 15 балів є показаннями до ревізійної операції на протезованому колінному суглобі.
На основі роботи пропонується вдосконалена система рентген-функціональної оцінки результату ендопротезування, що дозволяє об’єктивувати оцінку результату ревізій.
Висновки
1. Встановлено наступні вірогідні фактори ризику, що вплинули на нестабільність компонентів ендопротеза колінного суглоба: важка фізична праця (t = 1,34 і вище, р < 0,05); ожиріння зі значенням ІМТ ≥ 30 (t = 2,24 і вище, р < 0,05), залишкова деформація (хi2 = 4,55, n = 2, р < 0,05); ранні післяопераційні ускладнення (Z = 7,25, p < 0,01), порушення техніки цементування стегнового (t = 1,63 і вище, р < 0,05) та великогомілкового компонентів (t = 1,36 і вище, р < 0,05).
2. Встановлено ранні фактори, що впливають на результати ендопротезування колінного суглоба: резорбція кісткової тканини на межі «цемент — кістка», що проявляється у вигляді смужки просвітлення з локалізацією в 1, 2, 3, 4-й зонах (за Hyojeong Mulcahy і Felix S. Chew) як дистального відділу стегнової (t = 4,95 і вище, р < 0,05), так і проксимального відділу великогомілкової кістки (t = 1,52 і вище, р < 0,05).
3. Визначено пізні вірогідні фактори, що впливають на результати ендопротезування колінного суглоба. Домінуючими є зміни на межі як «цемент — кістка», так і «імплант — цемент», з локалізацією в «зонах виступів», а саме 5, 6, 7 (за Hyojeong Mulcahy і Felix S. Chew), що можуть трактуватись як пізні діагностичні критерії нестабільності компонентів ендопротезів колінного суглоба з цементним типом фіксації стегнового (t = 1,63 і вище, р < 0,05) та великогомілкового компонентів (t = 1,36 і вище, р < 0,05) .
4. Визначено, що з усіх випадків розхитування компонентів вірогідну більшість (t = 9,5 і вище, р < 0,05) становили випадки нестабільності з повним обсягом рухів в оперованому суглобі, а саме 63 випадки, що становило 74,1 %. Встановлений характер домінування свідчить про те, що порушення обсягу рухів у протезованому суглобі в сагітальній площині в післяопераційному періоді не має негативного впливу на розвиток нестабільності компонентів.
5. Визначені ранні рентгенологічні ознаки нестабільності (ознаки лізису стегнової та великогомілкової кісток в зонах 1 та 2 за Hyojeong Mulcahy і Felix S. Chew у поєднанні з динамічною пробою на нестабільність та УЗД-критеріями розхитування ендопротеза (ознаки гіперваскуляризації, синовіт з об’ємом рідини понад 50 см3 та позитивна динамічна проба).
6. На основі вивчених даних запропонована вдосконалена рентген-функціональна система оцінки протезованого суглоба та визначені оптимальні критерії діагностики розхитування компонентів і показання до своєчасної ревізії (зниження бальної оцінки менше ніж 15 балів).
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.
Отримано/Received 08.04.2024
Рецензовано/Revised 19.04.2024
Прийнято до друку/Accepted 28.04.2024
Список литературы
1. Steinhaus, M.E., Christ, A.B., & Cross, M.B. (2017). Total Knee Arthroplasty for Knee Osteoarthritis: Support for a Foregone Conclusion? HSS journal: the Musculoskeletal Journal of Hospital for Special Surgery, 13(2), 207-210. https://doi.org/10.1007/s11420-017-9558-4.
2. Ahmad Hafiz, Z., Masbah, O., Orth, & Ruslan, G.N. (2011). Total Knee Replacement: 12 Years Retrospective Review and Experience. Malaysian Orthopaedic Journal, 5, 34-39.
3. Pietrzak, J., Common, Н., Migaud, H., Pasquier, G., Girard, I., Putman, S. (2019). Have the frequency of and reasons for revision total knee arthroplasty changed since 2000? Comparison of two cohorts from the same hospital: 255 cases (2013–2016) and 68 cases (1991–1998). Orthopaedics & Traumatology: Surgery & Research, 105, Iss 4, 639-645. https://doi.org/10.1016/j.otsr.2019.01.025.
4. Lewis, P.L., Robertsson, O., Graves, S.E., Paxton, E.W., Prentice, H.A., & W-Dahl, A. (2021). Variation and trends in reasons for knee replacement revision: a multi-registry study of revision burden. Acta Оrthopaedica, 92(2), 182-188. https://doi.org/10.1080/17453674.2020.1853340.
5. Martinez, R., & Chen, A.F. (2023). Outcomes in revision knee arthroplasty: Preventing reoperation for infection Keynote lecture — BASK annual congress 2023. The Knee, 43, A5-A10. https://doi.org/10.1016/j.knee.2023.07.010.
6. Gallo, J., Goodman, S.B., Konttinen, Y.T., Wimmer, M.A., & Holinka, M. (2013). Osteolysis around total knee arthroplasty: a review of pathogenetic mechanisms. Acta biomaterialia, 9(9), 8046-8058. https://doi.org/10.1016/j.actbio.2013.05.005.
7. Chen, K., Xu, J., Dai, H., Yu, Y., Wang, Y., Zhu, Y., Tao, T., & Jiang, Y. (2023). Uncemented Tibial Fixation Has Comparable Prognostic Outcomes and Safety Versus Cemen–ted Fixation in Cruciate-Retaining Total Knee Arthroplasty: A Meta-Analysis of Randomized Controlled Trials. Journal of Clinical Medicine, 12(5), 1961. https://doi.org/10.3390/jcm12051961.
8. Kim, Y.H., Park, J.W., Kim, J.S. et al. (2014). The relationship between the survival of total knee arthroplasty and postoperative coronal, sagittal and rotational alignment of knee prosthesis. International Orthopaedics (SICOT), 38, 379-385. https://doi.org/10.1007/s00264-013-2097-9.
9. Kim, K.T., Lee, S., Kim, T.W., Lee, J.S., & Boo, K.H. (2012). The influence of postoperative tibiofemoral alignment on the clinical results of unicompartmental knee arthroplasty. Knee Surgery & Related Research, 24(2), 85-90. https://doi.org/10.5792/ksrr.2012.24.2.85.
10. Vasso, M., Braile, A., Ascione, F., Toro, G., De Cicco, A., Lepore, F., & Schiavone Panni, A. (2019). Two-stage reimplantation in periprosthetic knee infection. European Review for Medical аnd Pharmacological Sciences, 23(2 Suppl), 51-58. https://doi.org/10.26355/eurrev_201904_17474.
11. Lequesne, M.G. (1997). The algofunctional indices for hip and knee osteoarthritis. J. Rheumat, 24, 779-781. PMID: 9101517.
12. Cassar-Gheiti, A.J., McColgan, R., Kelly, M., Cassar-Gheiti, T.M., Kenny, P., & Murphy, C.G. (2020). Current concepts and outcomes in cemented femoral stem design and cementation techniques: the argument for a new classification system. EFORT Open Reviews, 5(4), 241-252. https://doi.org/10.1302/2058-5241.5.190034.
13. Mulcahy, H., Chew, F.S. (2014). Current Concepts in Knee Replacement: Complications. American Journal of Roentgenology, 202, 76-86. doi: 10.2214/AJR.13.11308.
14. Gaulrapp, H., & Eckstein, S. (2001). Der Wert der Sonographie nach endoprothetischer Versorgung des Kniegelenks [Value of ultrasound after endoprosthesis implantation of the knee joint]. Zeitschrift fur Orthopadie und ihre Grenzgebiete, 139(2), 127-133. https://doi.org/10.1055/s-2001-15043.
15. Engh, G.A., Rorabeck C.H. (1997). Revision total knee arthroplasty. Philadelphia: Lippincott-Raven. 459 р.
16. Berenbaum, F., Griffin, T.M., Liu-Bryan, R. (2017). Metabolic Regulation of Inflammation in Osteoarthritis. Arthritis Rheum, 69(1), 9-21.
17. Gunst, S., & Fessy, M.H. (2015). The effect of obesity on mechanical failure after total knee arthroplasty. Annals of Translational Medicine, 3(20), 310. https://doi.org/10.3978/j.issn.2305-5839.2015.10.37.
18. Lim, J.B., Loh, B., Chong, H.C., & Tan, A.H. (2016). History of previous knee surgery does not affect the clinical outcomes of primary total knee arthroplasty in an Asian population. Annals of Translational Medicine, 4(16), 303. https://doi.org/10.21037/atm.2016.08.15.
19. Bozic, K.J., Lau, E., Ong, K., Chan, V., Kurtz, S., Vail, T.P., Rubash, H.E., & Berry, D.J. (2014). Risk factors for early revision after primary TKA in Medicare patients. Clinical Orthopaedics аnd Related Research, 472(1), 232-237. https://doi.org/10.1007/s11999-013-3045-0.
20. Sharkey, P.F., Lichstein, P.M., Shen, C., Tokarski, A.T., & Parvizi, J. (2014). Why are total knee arthroplasties failing today — has anything changed after 10 years? The Journal of Аrthroplasty, 29(9), 1774-1778. https://doi.org/10.1016/j.arth.2013.07.024.
/34.jpg)

/33.jpg)
/35.jpg)
/36.jpg)
/37.jpg)