Международный неврологический журнал Том 21, №1, 2025
Вернуться к номеру
Оцінка клінічної ефективності та переносимості оригінального та генеричного еторикоксибу у пацієнтів з болем у нижній частині спини
Авторы: Тріщинська М.А. (1), Ханенко Н.В. (1), Бігун І.Ю. (1, 2), Інгула Н.І. (2), Антюк В.М. (2), Барна І.Б. (2), Борисова В.Л. (2), Невгад Ю.В. (2), Романенко І.П. (2), Шеремет А.Є. (2)
(1) - Національний університет охорони здоров’я України імені П.Л. Шупика, м. Київ, Україна
(2) - КНП «Київська обласна клінічна лікарня», м. Київ, Україна
Рубрики: Неврология
Разделы: Клинические исследования
Версия для печати
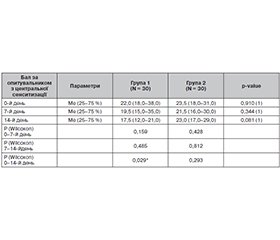
Актуальність. Біль у спині є однією з найбільш поширених скарг серед дорослого населення будь-якого віку та соціально-економічного статусу. За даними ВООЗ, до 80 % людей стикаються з цим станом хоча б раз у своєму житті. Найбільш поширеною локалізацією болю є нижня частина спини (low back pain). Мета: проаналізувати взаємозв’язки між ефективністю, ступенем полегшення симптомів та динамікою гострого неспецифічного механічного больового синдрому в нижній частині спини у пацієнтів з дегенеративними захворюваннями хребта залежно від вибраного лікування оригінальним або генеричним нестероїдним протизапальним препаратом. Матеріали та методи. У дослідження було включено 60 осіб з гострим больовим синдромом в нижній частині спини на фоні дегенеративних захворювань хребта, в тому числі спондильозу, остеоартрозу хребта, наявності гриж дисків, стенозу хребтового каналу, порушення статики хребта, які зверталися за амбулаторною та стаціонарною допомогою до невролога. Усі пацієнти випадковим чином (кожний другий) були розподілені на дві групи для лікування оригінальним чи генеричним еторикоксибом — нестероїдним протизапальним препаратом, що селективно блокує ЦОГ-2. Результати. Оцінка вираженості больового синдрому в нижній частині спини за візуальною аналоговою шкалою свідчить про те, що пацієнти обох груп на момент початку дослідження статистично значущо не різнилися за цим показником. На 7-й день лікування різниця між групами була статистично не значуща, але на 14-й день зниження болю в групі 1 було суттєво більшим — до рівня 5 балів проти зниження до рівня 20 балів у групі 2 (р < 0,001). Оцінка динаміки вираженості нейропатичного компонента болю за опитувальником painDETECT свідчить про те, що на початковому етапі групи мали статистично значущу різницю за рахунок більш вираженої (вищої) оцінки в групі 1 — 15 балів проти 11,5 бала у групі 2. На 7-й і 14-й день різниця між групами була статистично не значуща (групи були співставні), але на 14-й день зниження болю в групі 1 було дещо більш суттєвим — до рівня 2 балів проти зниження до рівня 3 балів у групі 2. Динаміка показника painDETECT була статистично значущою в обох групах (р < 0,001) з 0-го до 14-го дня лікування. Не було виявлено суттєвої різниці між пацієнтами груп за ознаками центральної сенситизації (відповідно до оцінки за опитувальником з центральної сенситизації) в окремі періоди спостереження (групи співставні). Проте у групі 2 показник сенситизації залишався практично незмінним за період дослідження, а в групі 1 спостерігалося поступове зниження показника, різниця якого за період з 0-го до 14-го дня досягла статистичної значимості (р = 0,029) — з 22 до 17,5 бала. Висновки. Вибір оригінального еторикоксибу в дозі 90 мг для застосування протягом 14 днів вірогідно і прогнозовано мав кращу ефективність та переносимість відносно генеричної молекули.
Background. Back pain is one of the most common complaints among adults of all ages and socioeconomic status. According to the World Health Organization, up to 80 % of people experience this condition at least once in their lives. The most common location of pain is the low back. Purpose of the study: to analyze the relationships between the effectiveness, degree of symptom relief and dynamics of acute nonspecific mechanical pain syndrome in the low back in patients with vertebral degenerative diseases, depending on the selected treatment with the original or generic nonsteroidal anti-inflammatory drug. Materials and methods. The study included sixty people with acute low back pain syndrome on the background of vertebral degenerative diseases, including spondylosis, vertebral osteoarthritis, the presence of herniated discs, spinal stenosis, violations of the statics of the spine. All patients were randomly (every other) divided into two groups for treatment with original or generic etoricoxib, a nonsteroidal anti-inflammatory drug that selectively inhibits cyclooxygenase-2. Results. Assessment of the severity of low back pain syndrome on the visual analog scale shows that the patients of both groups at the beginning of the study did not differ statistically significantly. On day 7 of treatment, the difference between the groups was not statistically significant, but on day 14, the pain reduction in group 1 was significantly greater — to the level of 5 points, compared with a reduction to 20 points in group 2 (p < 0.001). Assessing the dynamics of the neuropathic pain component severity using the painDETECT questionnaire shows that at the initial stage, the groups had a statistically significant difference due to a more pronounced (higher) score in group 1 — 15 points versus 11.5 points in group 2. On days 7 and 14, the difference between the groups was not statistically significant (the groups were comparable), but on day 14, the reduction in pain in group 1 was somewhat more significant, to the level of 2 points versus the reduction to the level of 3 points in group 2. The dynamics of the painDETECT indicator was statistically significant in both groups (p < 0.001) from day 0 to day 14 of treatment. No significant difference was found between the groups in terms of central sensitization (as assessed by the central sensitization questionnaire) during separate observation periods (the groups were comparable). However, in group 2, the sensitization index remained practically unchanged during the study period, and in group 1, it decreased gradually, the difference for the period from days 0 to day 14 reached statistical significance (p = 0.029), from 22 to 17.5 points. Conclusions. The choice of the original etoricoxib at a dose of 90 mg for use for 14 days reliably and predictably had better efficacy and tolerability compared to the generic molecule.
біль у нижній частині спини; дегенеративні зміни в хребті; гострий біль; неспецифічний механічний больовий синдром; ноцицептивний біль; нейропатичний біль; нестероїдний протизапальний засіб; оригінальний еторикоксиб; генеричний еторикоксиб
low back pain; vertebral degenerative changes; acute pain; nonspecific mechanical pain syndrome; nociceptive pain; neuropathic pain; nonsteroidal anti-inflammatory drug; original etoricoxib; generic etoricoxib