Журнал «Медицина неотложных состояний» Том 21, №6, 2025
Вернуться к номеру
Використання ад’ювантів у профілактиці рикошетного болю у пацієнтів, які отримали військову травму: проспективно-пілотне дослідження
Авторы: Ткачук М.М.1, Дмитрієв Д.В.2–4
(1) - ОКНП «Чернівецька лікарня швидкої медичної допомоги», м. Чернівці, Україна
(2) - Вінницький національний медичний університет імені М.І. Пирогова, м. Вінниця, Україна
(3) - Центр лікування болю та реабілітації «Прометей», м. Вінниця, Україна
(4) - Центр термічної травми та пластичної хірургії, Вінницька обласна клінічна лікарня імені М.І. Пирогова, м. Вінниця, Україна
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
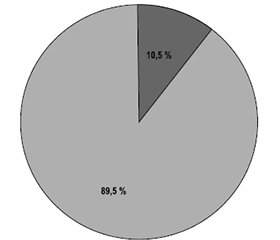
Рикошетний біль (РБ) — це гостре посилення післяопераційного болю після завершення дії блока периферичного нерва (PNB), що виникає у 30–60 % пацієнтів після одноразових регіонарних блокад, особливо при ортопедичних і травматичних втручаннях. У пацієнтів із бойовими травмами феномен рикошетного болю є особливо клінічно значущим, адже може ускладнювати перебіг реабілітації, знижувати толерантність до болю та підвищувати ризик розвитку нейропатичного компонента. Метою цього проспективного пілотного дослідження було оцінити ефективність дексаметазону як ад’юванта у складі одноразової блокади периферичного нерва у пацієнтів із бойовими пораненнями кінцівок. До дослідження було залучено 74 чоловіки віком від 22 до 45 років (середній вік 30,8 ± 4,7 року). Усі пацієнти були розподілені на дві групи: група 1 (n = 36) отримувала сингл-шот блокаду бупівакаїном (1,5–2 мг/кг); група 2 (n = 38) — бупівакаїн у комбінації з дексаметазоном 2 мг. Інтенсивність болю оцінювали за ВАШ через 6 і 12 годин після блокади. У групі 1 середній бал за ВАШ через 12 год становив 6,1, тоді як у групі 2 — 4,2. Частка пацієнтів із болем ≥ 7 балів хоча б в один момент становила 30,6 % (11 із 36) у групі 1 проти 13,1 % (5 із 38) у групі 2. Більше того, лише один пацієнт у групі 2 (2,6 %) мав ≥ 7 балів саме через 12 год після блокади, що свідчить про меншу вираженість РБ. Через 14 днів у групі 2 додатково проводилось оцінювання за шкалою DN4. 89,4 % пацієнтів (34 із 38) мали сумарний бал < 4, що вказує на відсутність нейропатичного болю, а у 10,6 % (4 пацієнти) ризик виявився підвищеним (DN4 ≥ 4). Середній бал за DN4 становив 2,1 ± 0,9, що свідчить про слабкий ступінь нейропатичних симптомів навіть у наявних випадках. Отримані результати демонструють, що додавання дексаметазону до місцевого анестетика при одноразовій блокаді значно зменшує інтенсивність рикошетного болю, знижує частку його тяжких форм і потенційно запобігає розвитку нейропатичного болю. Біологічна доцільність використання дексаметазону пояснюється його протизапальними властивостями, стабілізацією мембран, зменшенням периферичної сенситизації та потенціалом до пролонгації дії місцевих анестетиків. Незважаючи на обмеження дослідження (невелика вибірка, відсутність DN4 в обох групах), результати є обнадійливими та підкреслюють доцільність подальших рандомізованих досліджень із включенням катетерних методик, мультимодальної аналгезії та аналізу інших ад’ювантів.
Rebound pain (RP) is a sharp exacerbation of post-operative pain that occurs after the resolution of a peripheral nerve block (PNB). It is reported in 30–60 % of patients following single-injection regional blocks, particularly after orthopedic and traumatic surgeries. In patients with combat-related injuries, rebound pain is of particular clinical concern as it can complicate rehabilitation, reduce pain tolerance, and increase the risk of neuropathic pain development. The aim of this prospective pilot study was to evaluate the effectiveness of dexamethasone as an adjuvant to a single-shot PNB in patients with combat-related limb injuries. A total of 74 male patients aged 22–45 (mean of 30.8 ± 4.7) years were enrolled and divided into two groups. Group 1 (n = 36) received a single-shot bupivacaine block (1.5–2 mg/kg). In group 2 (n = 38), bupivacaine was combined with 2 mg of dexamethasone. Pain intensity was assessed using the Visual Analogue Scale (VAS) at 6 and 12 hours post-block. At 12 hours, the mean VAS score in group 1 was 6.1 compared to 4.2 in group 2. The proportion of patients experiencing pain
≥ 7 at any time point was 30.6 % (11 of 36) in group 1 versus 13.1 % (5 of 38) in group 2. Notably, only one patient (2.6 %) in group 2 reported a VAS score of ≥ 7 at 12 hours, indicating a significantly lower severity of RP. In group 2, DN4 assessment was performed additionally on day 14. 89.4 % of patients (34 of 38) had a DN4 score < 4, suggesting the absence of neuropathic pain, and 10.6 % (4 people) had an increased risk (DN4 scores ≥ 4). The mean DN4 score was 2.1 ± 0.9, reflecting mild neuropathic symptoms even in positive cases. The results demonstrate that adding dexamethasone to a local anesthetic in single-shot nerve blocks significantly reduces the intensity of rebound pain, the proportion of severe pain cases, and the risk of neuropathic progression. The biological rationale of dexamethasone use includes its anti-inflammatory effects, membrane stabilization, reduction of peripheral sensitization, and potential to prolong local analgesia. Despite certain limitations (small sample size, absence of DN4 data in group 1), this study provides encouraging findings that support further randomized trials involving larger cohorts, catheter-based techniques, multimodal analgesia, and alternative adjuvants.
рикошетний біль; регіонарна анестезія; дексаметазон; військова травма; DN4; ВАШ
rebound pain; regional anesthesia; dexamethasone; combat trauma; DN4; Visual Analogue Scale
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- Ahmed HM, Atterton BP, Crowe GG, et al. Recommendations for effective documentation in regional anesthesia: an expert panel Delphi consensus project. Reg Anesth Pain Med. 2022 May;47(5):301-308. doi: 10.1136/rapm-2021-103136.
- Dobrovanov O, Dmytriiev D, Prochotsky A, Vidiscak M, Furkova K. Pain in COVID-19: Quis est culpa? Electron J Gen Med. 2023;20(1):em435. doi: 10.29333/ejgm/12672.
- Dobrovanov O, Dmytriiev D, Prochotsky A, Vidiscak M, Furkova K. Chronic pain in post-COVID syndrome. Bratisl Lek Listy. 2023;124(2):97-103. doi: 10.4149/BLL_2023_014.
- Stone A, Lirk P, Vlassakov K. Rebound Pain After Peripheral Nerve Blockade-Bad Timing or Rude Awakening? Anesthesiol Clin. 2022 Sep;40(3):445-454. doi: 10.1016/j.anclin.2022.03.002.
- Gao M, Li Y, Yu J, et al. The Effects of Intravenous Dexamethasone on Rebound Pain After Nerve Block in Patients with Ankle Fracture: A Randomized Controlled Trial. J Pain Res. 2023 Mar 31;16:1127-1136. doi: 10.2147/JPR.S399660.
- Lee HJ, Woo JH, Chae JS, Kim YJ, Shin SJ. Intravenous versus perineural dexamethasone for reducing rebound pain after interscalene block in shoulder surgery: A randomized controlled trial. J Korean Med Sci. 2023;38(24):e183. doi: 10.3346/jkms.2023.38.e183.
- Bhatia P, Metta R. Rebound pain: Undesired, yet unexplored. J Anaesthesiol Clin Pharmacol. 2022 Oct-Dec;38(4):527-528. doi: 10.4103/joacp.joacp_435_22.
- Barry GS, Bailey JG, Sardinha J, Brousseau P, Uppal V. Factors associated with rebound pain after peripheral nerve block for ambulatory surgery. Br J Anaesth. 2021 Apr;126(4):862-871. doi: 10.1016/j.bja.2020.10.035.
- Muoz-Leyva F, Cubillos J, Chin KJ. Managing rebound pain after regional anesthesia. Korean J Anesthesiol. 2020 Oct;73(5):372-383. doi: 10.4097/kja.20436.
- Streb T, Schneider A, Wiesmann T, et al. Rebound pain — From definition to treatment. Anaesthesiologie. 2022 Aug;71(8):638-645. German. doi: 10.1007/s00101-022-01120-z.