Журнал «Медицина неотложных состояний» Том 21, №6, 2025
Вернуться к номеру
Церебральний венозний тромбоз: сучасний менеджмент і презентація клінічного випадку
Авторы: Дубенко О.Є. (1, 2), Гребенюк Г.В. (1, 3), Гаврюшин О.Ю. (3), Кириленко Є.І. (3), Анисєнкова В.Ю. (1, 3)
(1) - Харківський національний медичний університет, м. Харків, Україна
(2) - ДУ «Інститут медичної радіології та онкології імені С.П. Григор’єва НАМН України», м. Харків, Україна
(3) - КНП «Міська багатопрофільна лікарня № 18» ХМР, м. Харків, Україна
Рубрики: Медицина неотложных состояний
Разделы: Справочник специалиста
Версия для печати
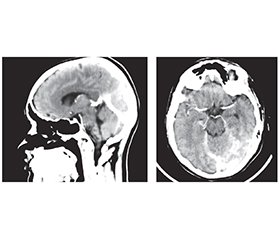
Церебральний венозний тромбоз є достатньо рідкісним типом порушення мозкового кровообігу і являє собою наявність тромбу у венозних синусах твердої оболонки й венах головного мозку. Церебральний венозний тромбоз найчастіше зустрічається у пацієнтів молодого віку, здебільшого у жінок. Фактори ризику церебральних венозних тромбозів можуть бути транзиторними або хронічними. До ключових належать статево-специфічні гормональні зміни: пероральна контрацепція і гормональна (переважно естрогенна) терапія, вагітність, інфекції, дегідратація, онкологічні, гематологічні й автоімунні захворювання. Найпоширеніший симптом тромбозу венозних синусів — інтенсивний головний біль, що є відображенням розвитку внутрішньочерепної гіпертензії; іншими симптомами можуть бути: фокальний неврологічний дефіцит, епілептичні напади, втрата або зміна свідомості до коми, порушення зору, менінгеальний синдром. Магнітно-резонансна томографія і магнітно-резонансна венографія є найбільш точними й високочутливими методами діагностики тромбозу церебральних венозних синусів, однак для підвищення вірогідності діагностики слід зважати і на результати інших методів дослідження, включно з комп’ютерною томографією і КТ-ангіографією. Тромби присутні у вигляді дефектів наповнення. Частота рецидивів тромбозів венозних синусів коливається від 1 до 4 % на рік, але вищий ризик може бути в осіб із тяжкою тромбофілією, включно зі злоякісними новоутвореннями. Лікування гострої стадії починається з парентерального введення низькомолекулярних гепаринів із подальшим переходом до пероральних антикоагулянтів протягом 3–12 місяців для посилення реканалізації та запобігання рецидиву. Жінкам із тромбозом церебральних венозних синусів у зв’язку із застосуванням комбінованих гормональних контрацептивів або вагітністю слід утримуватися від продовження або поновлення гормональної контрацепції через підвищений ризик рецидиву. Ми також наводимо клінічний випадок протяжного тромбозу верхнього сагітального синуса з поширенням тромбу в лівий поперечний, сигмоподібний синуси та внутрішню яремну вену у молодої жінки на тлі прийому гормональних естрогенвмісних препаратів зі сприятливим результатом.
Cerebral venous thrombosis is a fairly rare type of cerebral circulatory disorder; there is a thrombus in the venous sinuses of the dura mater and veins of the brain. Cerebral venous thrombosis is most common in young patients, more often in women. Risk factors for cerebral venous thrombosis can be transient or chronic. The key ones include sex-specific hormonal changes: oral contraception and hormonal (mainly estrogen) therapy, pregnancy, infections, dehydration, cancer, hematologic and autoimmune diseases. The most common symptom of venous sinus thrombosis is intense headache, which is a reflection of the development of intracranial hypertension; other symptoms may be focal neurological deficit, epileptic seizures, loss or change of consciousness up to coma, visual impairment, meningeal syndrome. Magnetic resonance imaging and magnetic resonance venography are the most accurate and highly sensitive methods for diagnosing cerebral venous sinus thrombosis, but to increase the reliability of the diagnosis, the results of using other research methods should be taken into account such as computed tomography and computed tomography angiography. Thrombi are present in the form of filling defects. The recurrence rate of venous sinus thrombosis ranges from 1 to 4 % per year, but the risk may be higher in individuals with severe thrombophilia, as well as malignant neoplasms. Treatment of the acute phase begins with parenteral administration of low-molecular-weight heparins followed by a transition to oral anticoagulants for 3–12 months to enhance recanalization and prevent recurrence. Women with cerebral venous sinus thrombosis resulting from the use of combined hormonal contraceptives or pregnancy should refrain from continuing or resuming hormonal contraception due to an increased risk of recurrence. We also present a clinical case of extensive superior sagittal sinus thrombosis with the spread of the thrombus to the left transverse, sigmoid sinuses and internal jugular vein in a young woman on the background of taking hormonal estrogen-containing drugs, with a favorable outcome.
тромбоз венозних синусів; діагностика; нейровізуалізація; антикоагулянти; гормональні контрацептиви
venous sinus thrombosis; diagnosis; neuroimaging; anticoagulants; hormonal contraceptives
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- Alet M, Ciardi C, Alemn A, et al. Cerebral venous thrombosis in Argentina: clinical presentation, predisposing factors, outcomes and literature review. J Stroke Cerebrovasc Dis. 2020;29:105145. doi: 10.1016/j.jstrokecerebrovasdis.2020.105145. Crossref.
- Saposnik G, Bushnell Ch, Coutinho JM, еt al. Diagnosis and Management of Cerebral Venous Thrombosis: A Scientific Statement From the American Heart Association. 2024;55(3);e77-e90. doi: 10.1161/STR.0000000000000456.
- Getahun D, Nash R, Flanders WD, et al. Cross-sex hormones and acute cardiovascular events in transgender persons: a cohort study. Ann Intern Med. 2018;169:205-213. doi: 10.7326/m17-2785. Crossref. PubMed.
- Sayko O, Bohdan A, Malankevich J. Chronic headache as a clinical manifestation of cerebral venous sinus thrombosis. International Neurological Journal. 2021;17(1):50-54. doi: 10.22141/2224-0713.17.1.2021.226919.
- Duman T, Uluduz D, Midi I, et al. A multicenter study of 1144 patients with cerebral venous thrombosis: the VENOST study. J Stroke Cerebrovasc Dis. 2017;26:1848-1857. doi: 10.1016/j.jstrokecerebrovasdis.2017.04.020. Crossref. PubMed.
- Sanchez van Kammen M, Lindgren E, Silvis SM, et al. Late seizures in cerebral venous thrombosis. Neurology. 2020;95:e1716-e1723. doi: 10.1212/WNL.0000000000010576.
- Gasparini S, Neri S, Brigo F, et al. Late epileptic seizures following cerebral venous thrombosis: a systematic review and meta-analysis. Neurol Sci. 2022;43:5229-5236. doi: 10.1007/s10072-022-06148-y. Crossref.
- Klein P, Shu L, Nguyen TN, et al. Outcome prediction in cerebral venous thrombosis: the IN-REvASC Score. J Stroke. 2022;24:404-416. doi: 10.5853/jos.2022.01606.
- Hiltunen S, Putaala J, Haapaniemi E, Tatlisumak T. Long-term outcome after cerebral venous thrombosis: analysis of functional and vocational outcome, residual symptoms, and adverse events in 161 patients. J Neurol. 2016;263:477-484. doi: 10.1007/s00415-015-7996-9. Crossref. PubMed.
- Field T, Dizonno V, Almekhlafi MA, et al. SECRET Investigators. Study of Rivaroxaban in Cerebral Venous Thrombosis: a randomized controlled feasibility trial comparing anticoagulation with rivaroxaban to standard-of-care in symptomatic cerebral venous thrombosis. Stroke. 2023;54:2724-2736. doi: 10.1161/STROKEAHA.123.044113. Crossref. PubMed.
- Liu L, Jiang H, Wei H, et al. Risk factors of impaired employability after cerebral venous thrombosis. CNS Neurosci Ther. 2023;29:1086-1093. doi: 10.1111/cns.14083.
- Palazzo P, Agius P, Ingrand P, et al. Venous thrombotic recurrence after cerebral venous thrombosis: a long-term follow-up study. Stroke. 2017;48:321-326. doi: 10.1161/strokeaha.116.015294. Crossref. PubMed.
- Shu L, Bakradze E, Omran SS, et al. Predictors of recurrent venous thrombosis after cerebral venous thrombosis: analysis of the ACTION-CVT study. Neurology. 2022;99:e2368-e2377. doi: 10.1212/wnl.0000000000201122. Crossref.
- Dmytriw AA, Song JSA, Yu E, Poon CS. Cerebral venous thrombosis: state of the art diagnosis and management. Neuroradio-logy. 2018;60:669-685. doi: 10.1007/s00234-018-2032-2. Crossref.
- Ferro JM, Bousser MG, Canho P, et al. European Stroke Organization guideline for the diagnosis and treatment of cerebral venous thrombosis. Eur J Neurol. 2017;24:1203-1213. doi: 10.1111/ene.13381. Crossref. PubMed.
- van Dam LF, van Walderveen MAA, Kroft LJM, et al. Current imaging modalities for diagnosing cerebral vein thrombosis: a critical review. Thromb Res. 2020;189:132-139. doi: 10.1016/j.thromres.2020.03.011. Crossref.
- Alajmi E, Zung J, Duquet-Armand M, Coutinho JM, Mandell DM. Prevalence of venous infarction in patients with cerebral venous thrombosis: baseline diffusion-weighted MRI and follow-up MRI. Stroke. 2023;54:1808-1814. doi: 10.1161/STROKEAHA.122.042336. Crossref. PubMed.
- Ferro JM, Bendszus M, Jansen O, et al. Recanalization after cerebral venous thrombosis: a randomized controlled trial of the safety and efficacy of dabigatran etexilate versus dose-adjusted warfarin in patients with cerebral venous and dural sinus thrombosis. Int J Stroke. 2022;17:189-197. doi: 10.1177/17474930211006303.
- Khan M, Arauz A, Uluduz D, et al. VENOST Study Group. Predictors of mortality and functional out come in pregnancy and puerperium-related cerebral venous thrombosis. Cerebrovasc Dis. 2023;52:393-400. doi: 10.1159/000527155.
- Siegler JE, Shu L, Yaghi S, et al. Endovascular therapy for cerebral vein thrombosis: a propensity-matched analysis of anticoagulation in the treatment of cerebral venous thrombosis. Neurosurgery. 2022;91:749-755. doi: 10.1227/neu.0000000000002098.
- Weimar C, Beyer-Westendorf J, Bohmann F, et al. New re-commendations on cerebral venous and dural sinus thrombosis from the German consensus-based (S2k) guideline. Neurol. Res. Pract. 2024;6:23. doi: 10.1186/s42466-024-00320-9.